あなたの腸は大丈夫? リーキーガット症候群(理論編①)
みなさんの腸はお元気ですか? 腸の健康がおびやかされている、その一つの状態がリーキーガット症候群です。
今回は、腸や全身の健康を考える上で重要な
・リーキーガット症候群とは
・健康な腸の状態とは
について、基礎的な理論をお届けいたします。
分子栄養学で重要視する消化管(口腔内、胃や腸)の健康。
いくら良い栄養素を摂ったとしても、まずそれが消化・吸収されなければ、分子栄養学的な健康づくりに向けた出発が遅れてしまいます。まずは一緒に腸の健康について考えていきましょう。

国民の7割の腸がリーキーガット⁉
つい先日、多くの日本の皆さんの腸が危険にさらされている可能性があるというニュースがありました。
「ヘルスライフビジネス(2023年5月1日発行)」によれば、
「国民の約7割はリーキーガットの状態に陥っている可能性」
さらに「この数字は昨今のコロナ禍によるストレスでさらに増加している」ことが指摘されています。
リーキーガットとはどのような状態を指すでしょう。そして、リーキーガットになると何がどのように健康に影響してくるでしょうか。
今回は、リーキーガット症候群について4回シリーズでお送りする、その第1回です。
リーキーガット症候群(LGS:Leaky Gut Syndrome)とは
リーキーガット症候群(LGS:Leaky Gut Syndrome.以下、リーキーガットと略します)とは、粘膜バリアにすき間があき、バリア機能が低下して異物が血管などを通し体内に漏れ出てしまう状態のことです※1。
日本語では腸管壁侵漏症候群(Increased intestinal permeability)とも呼ばれます。リーキーガットは正式な疾患名ではなく、状態のことを意味しています※1。
リーキーガットは腸と全身に炎症を起こす?
リーキーガットが注目されている理由は、腸のバリア機能が低下することが腸や全身の炎症を引き起こし、それがさまざまな疾病や体調不良に関わるのではないかと考えられるようになっているからです。
リーキーガットとタイトジャンクション
リーキーガットに特に影響しているといわれているのが、腸の分子レベルでの粘膜上皮細胞のところの構造、タイトジャンクションです。
タイトジャンクションとは、腸が栄養素と水分を適切に取り込みながら病原体などの敵を見分けて捨てる、という高度な役割を可能にしている細胞の分子構造のひとつです※2。
このタイトジャンクションの破綻が、本来ならば通さないはずの細菌やウイルス、食事由来の大きな分子などを通してしまうことによって、炎症性疾患や自己免疫疾患、食物アレルギーなどに関わっているのではないかと考えられています※2、※3。
分子栄養学では、必要な栄養素を取り込みながら要らないものを排除するという高度なシステムを担う腸粘膜上皮細胞(以下、腸上皮細胞)に異常が起こることは、
・栄養素を取り込むための腸の健全なシステム(タイトジャンクション、トランスポーターなど)の破綻
につながり、栄養障害につながる可能性を考えます。なぜなら細胞は栄養素でできており、栄養障害が起こることは細胞の生まれ変わりの材料補充に影響するのではないか。そしてそれがさらに栄養障害をうむ悪循環に陥る可能性を考えるからです。
腸上皮細胞は生まれ変わりのスピードが速く、文献によって日数は多少異なりますが、だいたい1週間以内に新しく生まれ変わるといわれています※4、※5、※6。
腸は栄養素の消化・吸収、免疫を司る重要な臓器
リーキーガットを考えるにあたり、まずは正常な腸の働きについて一緒に考えましょう。
私たちの身体は食べた栄養素でできていますが、もっと的確な言い方をすると、腸を含む消化管で消化・吸収された栄養素がしっかりと代謝されたものでできています。
今回の話題の中心となる腸は、栄養素の消化・吸収を司る、健康な身体にとって欠かせないもっとも重要な臓器のひとつです。また、腸には身体全体の約6~7割の免疫細胞がすんでいるといわれ、毎日食べものや飲みものに付着して入ってくる病原体や有害物質などの異物を排除してくれる人体最大の免疫器官(腸管免疫)です。
正常な腸の主なシステム
リーキーガットに関わる点において、正常な腸の主なシステムとしては下記の4つが考えられます。
役割1:栄養素の消化・吸収
腸は、大まかに小腸と大腸に分けられ、私たちが食べる栄養素や水分を消化・吸収しています。
食事を口で噛み、飲み込んだ後、胃でさらに分解されます。小腸は胃に続く部分で、主に胃で分解された食物から栄養素を吸収する働きがあります。残ったものは大腸に送られ、小腸で吸収されなかった水分や栄養素などが吸収され、残ったものが最終的に肛門から便となって排泄されます。
役割2:免疫における物理的・化学的なバリア機能※7
腸の粘膜は免疫機能における第一の物理的バリアとして働いています(※感染と免疫の仕組みを知ろう「感染と免疫の基本」)。
外と接する腸の部分は、敵が入って来れないように粘膜ですきまなく覆われています。粘膜を構成する腸上皮細胞の中には、粘液層のねばねば(ムチン)や抗菌作用を発揮するペプチドを分泌してバリア機能をサポートしている細胞もいます※8。
粘膜を覆うねばねばの粘液層と、その下の粘膜上皮細胞層のところの腸上皮細胞と腸上皮細胞をぴったりとくっつけるタイトジャンクションなどの構造が物理的バリアの主体となります。
粘液の中には抗菌ペプチドなどが分泌されます。そしてそれが病原体などを排除して粘膜によるバリアを強化します(化学的バリア)※9、※10。粘液は物理的に異物を流して捨てるなどの大切な役割をしています。
役割3:免疫機能(腸管免疫)
小腸には「パイエル板」という、粘膜の真下にある袋状の構造(リンパ組織)があります。
パイエル板には、大量の樹状細胞、T細胞、B細胞などの免疫担当細胞(※免疫を司る白血球「白血球の仲間たちの基礎」)が大集合していて、腸粘膜にあるM細胞という特殊な細胞と連絡を取り合い、絶えずやってくる敵に負けないように備えています。そして粘液の中に大量の分泌型IgA抗体(以下、IgAと略します)を送り込んで敵の侵入を阻止しています※9。
IgAは粘膜のバリア機能をさらにサポートする役割をしています。粘膜の腸上皮細胞は、免疫担当細胞に自分のおなかにもともと棲んでいる細菌(共生細菌)や腸内病原体の合図(シグナル)を伝え、適切な腸管免疫をコントロールして腸の機能を正常に保つ機能を担っています※9。
役割4:腸内細菌叢のすむ場所を提供
人の腸には、たくさんの細菌が種類ごとに集まって存在しています。
人は腸内細菌に棲む場所を提供していますが、それらの腸内細菌はただ単にすむだけでなくビタミンを作ったり、食事として入ってくるプレバイオティクス(食物繊維など)を発酵して短鎖脂肪酸などをつくり出し、それが人の健康に役立つというお互いに利益を共有するWin-Winの関係にあります。
有用菌の作った短鎖脂肪酸(酪酸)は、腸粘膜を整え、腸のバリア機能をしっかり作ることにもつながることが報告されています※11。(※子供の栄養「腸は全身をコントロールする第2の脳」)
腸粘膜は、腸内細菌が免疫担当細胞に攻撃されることなく心地よくすみ続けてもらうために、それらのテリトリーを分け隔てるバリアとしての役割も担っています※9。
また無菌動物ではパイエル板の数が減って小さくなり、腸上皮細胞の入れ替わり(ターンオーバー)のスピードが低下するなど、腸の常在細菌の存在が腸の免疫組織の正常な発達に関わっていることが明らかになっています※12。
肥満、2 型糖尿病、非アルコール性脂肪肝(※年末年始に向けた正しい身体づくり「脂肪肝対策①」)では軽度な炎症が特徴として知られていますが、腸内細菌叢とその代謝産物の変化が、腸のバリア機能不全と全身性炎症を引き起こすことが示唆されています※13。
このように、腸の健康・恒常性は、腸上皮細胞、免疫担当細胞、腸内細菌叢がお互いに繊細かつ複雑に相互に作用し合うことによって維持されています。
リーキーガットを細胞レベルで考える
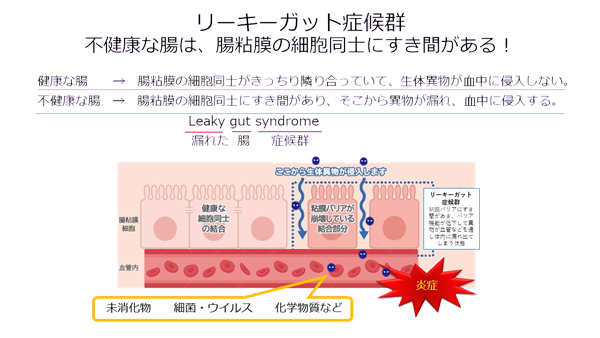
そんな大切な腸が危険にさらされているという状態のひとつがリーキーガットです。リーキーガットのイメージは、健康な腸にはないはずの小さなすき間がたくさん開いてしまっている状態です。それを細胞レベルで見てみるとこうなります。
私たちを構成するいちばん小さな “生きている単位” は細胞です。腸も細胞でできています。
健康な腸の内側を覆うのは粘膜(※感染と免疫の仕組みを知ろう「感染と免疫の基本」)です。腸の粘膜は、一層の腸上皮細胞という細胞でできた層と、その層を覆うぬるぬるした粘液層、腸上皮細胞層の下に続く免疫・血管などを含む粘膜固有層とよばれる層などで構成されています。
健康な腸の表面にある粘膜は、隣り合った腸上皮細胞同士がぴったりとくっついて必要なものだけを取り込み、それ以外の異物が血液中に侵入できないような1枚のシートのようになっています。
一方 不健康な腸は、隣り合った細胞同士の間にすき間があき、バリア機能が低下してそこから異物が漏れ血液中などを通して体内に侵入してしまう、いわば「ざる」のような状態です。この、腸(gut)から異物が漏れている(leaky)状態がリーキーガットです。

次回、※あなたの腸は大丈夫? リーキーガット症候群(理論編②)では、リーキーガット症候群についてさらに詳しく説明しています。ご参照ください。
(※第2回:あなたの腸は大丈夫? リーキーガット症候群(理論編②))
(※第3回:分子栄養学的リーキーガット症候群対策①(プレバイオティクス・プロバイオティクス編))
(※第4回:分子栄養学的リーキーガット症候群対策②(生活習慣・栄養素対策編)))
※1 和田孝一郎.リーキーガット症候群(Leaky Gut Syndrome)と疾患-NASH発症との関連性を中心として-.島根医学, 40(3):147-156.(2020) ※2 Suzuki T. Regulation of intestinal epithelial permeability by tight junctions. Cellular and Molecular Life Sciences, 70 : 631–659 (2013) ※3 Kinashi Y.,et al. Partners in Leaky Gut Syndrome: Intestinal Dysbiosis and Autoimmunity.Frontiers in Immunology, 12:673708.(2021) ※4 Sato T.,et al. Single Lgr5 stem cells build crypt-villus structures in vitro without a mesenchymal niche. Nature, 14;459(7244):262-265.(2009) ※5 van der Flier LG.,et al. Stem cells, self-renewal, and differentiation in the intestinal epithelium. Annual Review of Physiology, 71:241–260. (2009) ※6 Luissint AC.,et al. Inflammation and the Intestinal Barrier: Leukocyte–Epithelial Cell Interactions, Cell Junction Remodeling, and Mucosal Repair. Gastroenterology,151(4): 616–632.(2016) ※7 Bischoff C.S.,et al., Intestinal permeability – a new target for disease prevention and therapy. BMC Gastroenterology, 14: 189. (2014) ※8 Belkaid Y.,et al. Homeostatic immunity and the microbiota. Immunity,46(4):562–576.(2017) ※9 PetersonW.L.,et al. Intestinal epithelial cells: regulators of barrier function and immune homeostasis. Nature Reviews Immunology,14(3):141-153.(2014) ※10 Chelakkot C.,et al. Mechanisms regulating intestinal barrier integrity and its pathological implications. Experimental & Molecular Medicine,50:1–9 (2018) ※11 Kelly C. J.,et al. Crosstalk between Microbiota-Derived Short-Chain Fatty Acids and Intestinal Epithelial HIF Augments Tissue Barrier Function. Cell Host Microbe, 17(5) :662-671.(2015) ※12 Round L.J. ,et al. The gut microbiome shapes intestinal immune responses during health and disease. Nature Reviews Immunology, 9(5): 313–323.(2009) ※13 Tilg H.,et al. The intestinal microbiota fuelling metabolic inflammation. Nature Reviews Immunology,20:40–54. (2020)